Vous avez peut-être remarqué que votre ordonnance change de nom : au lieu de Advil, vous voyez maintenant ibuprofène. Ou votre traitement pour l’hypertension passe d’Lisinopril à une version moins chère. Ce n’est pas une erreur. C’est l’approbation FDA des médicaments génériques en action. Et pourtant, beaucoup de patients se demandent : sont-ils vraiment pareils ? Sont-ils sûrs ? Pourquoi coûtent-ils si peu ? Voici ce que vous devez vraiment savoir, sans jargon ni complexité inutile.
Qu’est-ce qu’un médicament générique ?
Un médicament générique est la copie exacte d’un médicament de marque, mais sans le nom de marque. Il contient le même ingrédient actif, à la même dose, sous la même forme (comprimé, sirop, injection) et pour le même usage. Par exemple, le générique du Prozac s’appelle fluoxétine. La différence ? Le prix. Un générique coûte en moyenne 80 à 85 % moins cher que le médicament de marque. En 2023, 90 % des ordonnances aux États-Unis étaient pour des génériques - mais ils ne représentaient que 23 % des dépenses totales en médicaments.
Comment est-ce possible ? Parce que les fabricants de génériques n’ont pas à refaire les essais cliniques coûteux. Le médicament de marque a déjà prouvé qu’il était sûr et efficace. Le générique, lui, doit seulement prouver qu’il fonctionne de la même manière dans le corps. C’est ce qu’on appelle la bioéquivalence.
Comment la FDA valide un générique ?
Le processus s’appelle ANDA - demande d’approbation de médicament générique abrégée. C’est une voie rapide, mais très rigoureuse. Voici ce que chaque fabricant doit prouver :
- Même ingrédient actif : pas de variation. Si le médicament de marque contient 20 mg de atorvastatine, le générique doit en contenir exactement 20 mg.
- Même forme et voie d’administration : si le médicament est un comprimé avalé, le générique ne peut pas être une injection. Même si cela semble évident, certains fabricants essaient de contourner cette règle - et la FDA le bloque.
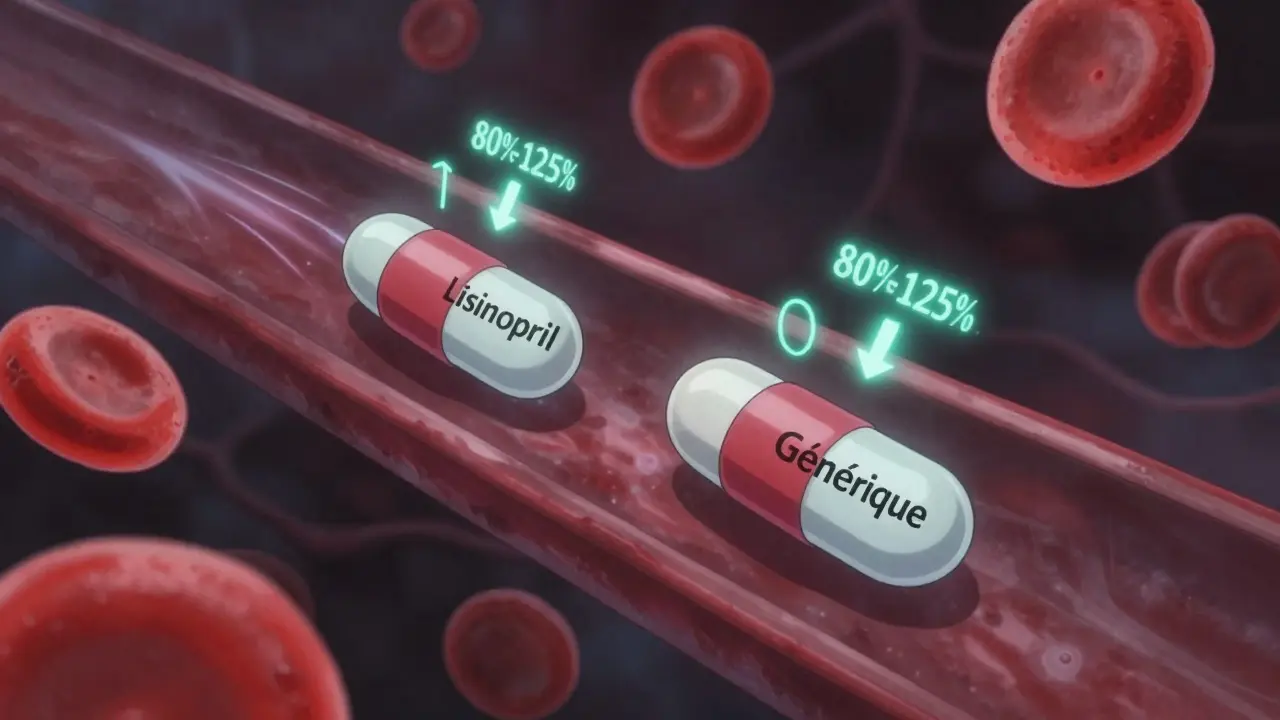
- Même performance dans le corps : c’est la clé. Les chercheurs donnent le générique et le médicament de marque à 24 à 36 volontaires en bonne santé. Ils mesurent combien de produit entre dans le sang, et à quelle vitesse. Le générique doit avoir entre 80 % et 125 % de la même quantité absorbée que le médicament original. C’est ce qu’on appelle le rapport de bioéquivalence.
- Même étiquetage : les instructions, avertissements et mises en garde doivent être identiques. Pas de surprises.
La FDA vérifie aussi les installations de fabrication. Chaque site doit respecter les normes cGMP - bonnes pratiques de fabrication. En 2022, l’agence a inspecté plus de 1 500 usines dans le monde pour s’assurer que les génériques soient produits dans des conditions sûres. Une usine qui ne respecte pas ces normes ne reçoit pas l’approbation.
Combien de temps ça prend ?
Le processus d’approbation d’un générique prend en moyenne 10 mois après le dépôt complet de la demande. Pour les médicaments simples, comme les comprimés d’ibuprofène ou de lévothyroxine, ça peut être plus rapide. Pour les produits complexes - comme les inhalateurs, les crèmes topiques ou les solutions ophtalmiques - ça peut prendre jusqu’à 24 mois ou plus. En 2023, les génériques complexes représentaient seulement 15 % des demandes, mais 40 % des retards d’approbation.
La FDA a lancé en 2023 une initiative spéciale pour accélérer l’approbation de ces médicaments difficiles. Le premier générique de l’EpiPen a été approuvé en septembre 2023, après 15 ans de tentatives. C’était un tournant majeur.
Pourquoi les génériques sont-ils si bon marché ?
Le coût de développement d’un médicament de marque peut atteindre 2,6 milliards de dollars. Pour un générique ? Entre 5 et 10 millions. Pas besoin de recherches initiales, pas besoin d’essais cliniques longs et coûteux. Les entreprises génériques se concentrent sur la fabrication, la validation et la soumission. Quand le brevet du médicament de marque expire, plusieurs fabricants peuvent entrer sur le marché. Cette concurrence fait chuter les prix.
En 2022, un seul médicament de marque a perdu son brevet - et 6,7 fabricants différents ont déposé une demande de générique. Résultat ? Le prix a chuté de 90 % en moins d’un an. C’est ce que la FDA appelle la « compétition générique ».
Les génériques sont-ils sûrs pour tout le monde ?
La réponse courte : oui. La FDA exige que les génériques soient aussi sûrs et efficaces que les médicaments de marque. Des millions de patients les prennent chaque jour sans problème.
Mais il y a une exception importante : les médicaments à indice thérapeutique étroit. Ce sont des traitements où une petite variation dans la dose peut causer des effets graves. Par exemple : la lévothyroxine (pour la thyroïde), le warfarin (anticoagulant), ou la cyclosporine (pour les transplantations). Pour ces médicaments, la FDA recommande de rester sur le même fabricant si possible. Certains patients rapportent des changements d’état après un passage d’un générique à un autre - même si les analyses scientifiques ne trouvent pas de différence significative.
Une étude de la FDA en 2022 a montré que 87 % des patients étaient satisfaits de leurs génériques. Mais 18 % des patients prenant des médicaments à indice étroit ont signalé des inquiétudes. Si vous faites partie de ce groupe, parlez-en à votre médecin ou pharmacien. Il peut vous aider à rester sur le même produit.
Qu’en est-il des « faux génériques » ?
Il n’existe pas de « faux génériques » approuvés par la FDA. Tous les génériques vendus légalement aux États-Unis doivent être approuvés. Mais certains produits en ligne ou importés prétendent être des génériques sans autorisation. Ces produits sont dangereux. Ils peuvent contenir trop peu ou trop d’ingrédient actif, ou même des substances toxiques. La FDA ne les surveille pas. Si vous achetez un médicament en ligne, assurez-vous qu’il provient d’une pharmacie américaine certifiée.

Comment savoir si votre médicament est générique ?
Regardez l’étiquette. Le nom du médicament doit être l’ingrédient actif (ex. : metformine), pas le nom de marque (ex. : Glucophage). Votre pharmacien peut aussi vous le dire. La FDA publie une liste publique appelée le Orange Book, qui contient tous les médicaments approuvés - marques et génériques. Vous pouvez la consulter en ligne gratuitement.
Que change le futur ?
La FDA travaille à améliorer le processus. D’ici 2025, elle prévoit d’utiliser l’intelligence artificielle pour analyser les demandes d’approbation plus rapidement. Elle veut aussi faciliter l’accès aux échantillons de médicaments de marque pour les fabricants de génériques - une pratique que certains laboratoires bloquent artificiellement pour retarder la concurrence.
En 2023, plus de 90 nouveaux génériques ont été approuvés. En 2024, des centaines d’autres suivront, car de nombreux médicaments coûteux perdent leurs brevets. Le marché des génériques devrait atteindre 150 milliards de dollars d’ici 2027. Pour les patients, cela signifie plus d’accès, plus de choix, et des économies importantes.
Que faire si vous avez des doutes ?
- Ne refusez pas un générique sans parler à votre médecin ou pharmacien.
- Si vous changez de générique et que vous sentez un changement (fatigue, étourdissements, effet réduit), notez-le et informez votre professionnel de santé.
- Utilisez toujours la même pharmacie si vous prenez un médicament à indice thérapeutique étroit.
- Ne payez jamais plus cher pour un générique que pour le médicament de marque - c’est rare, mais ça arrive.
Les génériques ne sont pas une version « moins bonne ». Ils sont la même chose, à un prix juste. La FDA les a vérifiés. Des millions de personnes les prennent. Et ils sauvent des vies - chaque jour.
Un médicament générique est-il aussi efficace qu’un médicament de marque ?
Oui. La FDA exige que les génériques aient la même efficacité, la même sécurité et la même qualité que les médicaments de marque. Ils doivent démontrer une bioéquivalence stricte : ils doivent libérer le même ingrédient actif dans le sang à la même vitesse et dans la même quantité. Des études sur des millions de patients montrent qu’ils fonctionnent de la même manière.
Pourquoi les génériques coûtent-ils moins cher ?
Les fabricants de génériques n’ont pas à repeindre les essais cliniques coûteux que le laboratoire de marque a déjà réalisés. Ils n’investissent pas non plus dans la publicité massive ou le marketing. Leur coût de développement est 100 fois moins élevé. Lorsque plusieurs entreprises produisent le même médicament, la concurrence fait chuter les prix.
Puis-je faire confiance aux génériques fabriqués à l’étranger ?
Oui, à condition qu’ils soient approuvés par la FDA. Les usines situées à l’étranger (en Inde, en Chine, en Corée, etc.) doivent respecter les mêmes normes de fabrication que celles aux États-Unis. La FDA inspecte régulièrement ces sites. Si un médicament est vendu légalement aux États-Unis, il a été vérifié, peu importe où il a été fabriqué.
Qu’est-ce qu’un médicament à indice thérapeutique étroit ?
C’est un médicament où une petite variation dans la dose peut avoir de graves conséquences. Exemples : la lévothyroxine (thyroïde), le warfarin (anticoagulant), la cyclosporine (transplantation). Pour ces médicaments, la FDA recommande de rester sur le même fabricant, car même de petites différences dans l’absorption peuvent affecter votre santé. Parlez à votre médecin si vous changez de générique.
Comment savoir si mon générique est approuvé par la FDA ?
Regardez l’étiquette : le nom du médicament doit être l’ingrédient actif (ex. : atenolol), pas un nom de marque. Votre pharmacien peut aussi le confirmer. Vous pouvez consulter la base de données publique du FDA appelée l’Orange Book, qui liste tous les médicaments approuvés - marques et génériques - avec leurs détails techniques.

Jean-Marc Frati
mars 18, 2026 AT 02:17Je viens de changer de générique pour mon traitement de la tension et j’ai pas senti la différence… mais j’ai économisé 80€ sur le mois. La FDA a raison : c’est la même pilule, juste sans le logo. Merci pour ce rappel clair !
mathilde rollin
mars 19, 2026 AT 14:01Je trouve ça incroyable qu’on puisse encore douter de la qualité des génériques. Ma mère prend de la lévothyroxine depuis 15 ans, toujours en générique, et elle va super bien. Les médecins qui disent le contraire n’ont pas lu les études.
nadine deck
mars 20, 2026 AT 01:42Je tiens à souligner que la bioéquivalence n’est pas un concept vague : elle repose sur des données statistiques rigoureuses, avec des intervalles de confiance à 90 % et des critères de non-infériorité. La FDA exige une AUC et une Cmax comprises entre 80 % et 125 %, ce qui garantit une variabilité biologique acceptable, pas une différence thérapeutique. Ce n’est pas un détail technique - c’est une norme mondiale.
cyril le boulaire
mars 21, 2026 AT 05:31Alors là, je rigole… vous croyez vraiment que les labos américains sont saints ? J’ai vu un générique qui sentait la pluie et le moisi. J’ai demandé à mon pharmacien, il m’a dit : "C’est normal, c’est fait en Inde." OK. Mais pourquoi on me le vend comme si c’était du luxe ?
Helder Lopes
mars 22, 2026 AT 05:31En Suisse, on a les mêmes règles. J’ai pris un générique pour mon cholestérol et j’ai vu mon compte bancaire respirer. C’est fou comment on a peur de l’économie… alors que ça sauve des vies. Merci pour cette explication simple et précise.
Guy COURTIEU
mars 23, 2026 AT 14:43Je viens de vérifier l’Orange Book… et là, j’ai vu que mon générique est fabriqué à Nantes. 😱
Floriane Jacqueneau
mars 24, 2026 AT 03:21Attention : certains génériques ont des excipients différents. Ce n’est pas anodin. J’ai une intolérance au lactose, et un générique m’a mis K.O. pendant deux semaines. Il faut lire les notices. Pas juste se fier à "même ingrédient actif".
Quentin Tridon
mars 24, 2026 AT 05:41Je suis allé dans un labo de génériques en Inde l’an dernier. Les machines sont plus modernes que chez certains labos français. On a des normes, mais pas de culture du contrôle qualité. Et pourtant, la FDA les inspecte. Donc oui, c’est fiable… mais c’est une chance, pas une certitude.
Juliette Forlini
mars 25, 2026 AT 19:31La FDA ? T’as vu comment ils ont caché les essais sur le Prozac ? Ils ont fait des tests sur des patients en surmédication pour prouver que le générique "fonctionnait". C’est un piège. Les labos paient les inspecteurs. Je connais quelqu’un qui a eu un AVC après un changement de générique… et personne n’en parle.
Guillaume Schleret
mars 26, 2026 AT 17:59Mon pharmacien m’a dit que je pouvais changer sans problème. J’ai fait. Rien changé. Et j’ai payé 30 € de moins. Simple.
Jean-Baptiste Chauvin
mars 28, 2026 AT 06:00je suis tombé sur un générique qui avait l'air d'un comprimé de céréale... mais bon, j'ai pas eu de problème. je suis pas un expert mais j'ai confiance dans la FDA. surtout que j'ai pas les moyens de payer 150€/mois pour un truc qui fait pareil.
Jacqueline Pedraza
mars 28, 2026 AT 17:54Je suis pharmacienne et je recommande toujours les génériques - sauf pour la lévothyroxine. Là, je dis aux patients : "Restez sur le même, même si c’est plus cher." Parce que même un 5 % de variation peut tout changer. La science dit oui, mais le corps, il a ses règles.